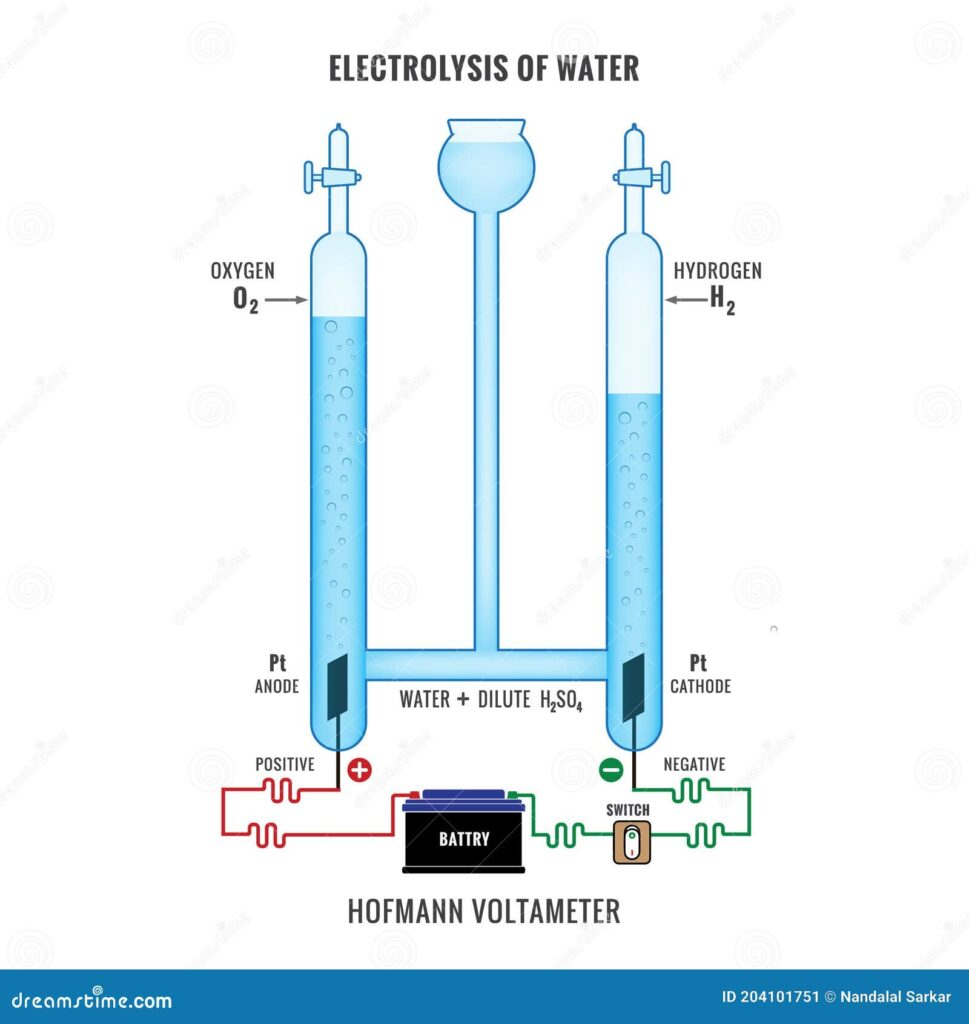
Электролиз воды
Считается, что впервые химический состав воды был определён французским химиком Лавуазье в 1784 году. Он, вместе с военным инженером Мёнье, прогонял пары воды над раскалённым листом железа. Они обнаружили, что вода разлагается, выделяя при этом водород и кислород. До этого времени вода считалась совершенно однородным веществом.
Предполагается, что авторитет Лавуазье помешал другим учёных заниматься поисками в этой области. Более того, это утвердило в умах многих поколений вывод о химическом составе воды.
С позиции сегодняшнего дня, можно сказать, что условия, при которых проводился опыт, были ужасными с точки зрения чистоты эксперимента. Железо, над которым пропускались пары воды способно внести многочисленные искажения в опыт. Их сложно учесть наперёд. Лавуазье и Мёнье зафиксировали выделение двух газов – водорода и кислорода. По какой-то причине, они посчитали маловажным то, что выделялись другие вещества.
Позже ряд учёных (Николсон, Кавендиш и др.) провели опыты по электрохимическому разложению воды. При электролизе воды выделялись водород и кислород. Они обнаружили два странных явления. Во-первых, обе составные части воды выделялись отдельно друг от друга. Кислород у одного электрода, водород – у другого. Во-вторых, наблюдалось образование кислоты у кислородного полюса и щёлочи у во-дородного.
Это «странное» разложение воды озадачило учёных. Но их больше безпокоила вторая «странность», т.е. появление кислоты и щелочи. Выделение водорода и кислорода вполне устраивало учёных. Это подтверждало ставшее уже господствующим мнение о составе воды.
Вопрос о том, каким образом эти составные части выделялись, при каких сопутствующих обстоятельствах – мало волновал учёных того времени. Их внимание было направлено главным образом на вторую «странность». Она вызывала сомнения в правильности формулы воды.
Выдающийся английский химик Гемфри Дэви решил разгадать эту загадку. Считается, что он подтвердил, что образование кислоты и щелочи при электролизе воды – случайное явление. Дэви проделал многочисленные опыты по «разложению» электричеством тщательно очищенной воды в различных сосудах: агатовых, стеклянных, сделанных из плавикового шпата, сернокислого барита и т.п. Он пытался максимально уменьшить влияние материала сосудов на результаты опытов.
Во всех опытах при электролизе воды он получал у анода сильную кислоту, у катода щёлочь. Дэви связывал это с тем, что чистая вода отчасти все же разлагала материал сосудов. Это и явилось причиной образования кислоты и щелочи. Важным следствием опытов было то, что количество образующихся у электродов кислоты и щелочи стояло в прямой зависимости от продолжительности опытов. Чем продолжительнее они были, тем больше образовывалось кислоты и щелочи и тем сильнее была их концентрация.
В опытах Дэви по электролизу различных растворов солей получалась аналогичная картина. У анода шло образование кислоты с выделением кислорода, у катода – образование щелочи с выделением водорода или чистого аммиака. Эти процессы должны были бы подтолкнуть его к выводам относительно общих закономерностей, относящихся к процессу электролиза.
При электролизе различных веществ, у электродов происходят окислительно-восстановительные процессы, вместо простого разложения веществ. Более того, только при наличии окислительно-восстановительного процесса может идти и сам электролиз. При этом реакция окисления происходит у одного электрода, а реакция восстановления у другого.
Было грубой ошибкой рассматривать электролиз как простой процесс разложения веществ на составляющие их элементы, будь то вода, соль или кислота. Окисление у одного полюса происходит при одновременном восстановлении у другого, и наоборот. Эти положения суть святая святых электрохимических процессов, полностью согласующихся со вторым началом термодинамики.
Примеры с электролизом солей показывают, что у анода происходила реакция восстановления с выделением кислорода (продуктом этой реакции, скапливающимся у анода, во всех случаях выступала какая-нибудь кислота). У катода происходила реакция окисления с выделением водорода или металла (продуктом этой реакции, скапливающимся у катода, всегда была какая-нибудь щёлочь).
Это должно распространяться и на воду. По какой-то причине, эта совершенно очевидная вещь отвергалась. Возможно, им помешали это сделать. У власть имущих имеется много возможностей для «убеждения».
Для того чтобы избежать всяких побочных влияний, Дэви провёл ряд опытов в золотых сосудах с хорошо очищенной водой. На протяжении четырнадцати часов количество кислоты в анодном сосуде постоянно возрастало. Дэви обнаружил, что она по своим свойствам похожа на азотную кислоту. Кислота образовывалась в опытах, проводимых им прежде в стеклянных сосудах. В катодном же сосуде образовывалась летучая щёлочь, количество которой скоро доходило до определённого предела. Она обнаруживала свойство аммиака (NH3).
Дэви повторил свой опыт и продолжал его без перерыва трое суток. К концу этого времени вода в сосудах была разложена и выпарилась больше чем на половину своего первоначального объёма. В результате, в анодном сосуде образовалась сильная азотная кислота, количество же щелочи оставалось примерно на том же уровне, как и в предыдущем опыте. Дэви посчитал, что последнее было связано с ее постоянным испарением.
Явные источники появления в опытах азота – отсутствовали. Дэви предположил, что образование азотной кислоты было обязано соединению водорода и кислорода в момент их выделения с азотом воздуха, который был растворён в воде. Для подтверждения своей догадки, он проделал тот же опыт под колоколом воздушного насоса, из которого он выкачал воздух. В итоге получились, в катодном сосуде в воде отсутствовала щёлочь. В анодном сосуде лакмусовая бумажка слабо окрасилась в красный цвет, что свидетельствовало об образовании там малого количества кислоты.
Казалось, его догадка подтверждалась. Чтобы уже окончательно убедиться в своей правоте, Дэви еще раз повторил свой опыт под колоколом, но теперь уже в атмосфере чистого водорода. При этом для большей чистоты опыта он дважды наполнял колокол водородом, чтобы удалить всякие остатки воздуха. В итоге – в сосудах отсутствовали даже следы щёлочи и кислоты.
Дэви допустил серьезную ошибку в своём первоначальном предположении. Он считал, что причиной образования кислоты и щелочи являлся азот воздуха. Азот в обычных условиях химически пассивен. Он отказывается растворяться в воде, вступать в реакции с кислородом и с водородом. Один этот факт должен был бы натолкнуть на поиски иных источников образования кислоты и щелочи.
Дэви удалось лишь создать условия, при которых во время электролиза воды перестали образовываться кислота и щёлочь. Они обязательно образуются в нормальных, естественных условиях. Получилась подгонка опытов под желаемый результат. Возможно, был такой заказ.
Предположим, что вода действительно состоит только из водорода и кислорода. Тогда естественно было бы предполагать, что, если вода с такой лёгкостью разлагается на свои составные части, она должна столь же легко образовываться в результате их синтеза. Всё в точности наоборот. Смесь одного объёма кислорода и двух – водорода даёт гремучий газ. Попытки образования воды из водорода и кислорода имели успех только в присутствии катализатора.
Вероятно, большинство опытов по определению химического состава воды было направлено на подгонку их результатов к уже имеющемуся выводу. Множество фактов биологического, химического и физического свойства доказывают, что существующая формула воды – ошибочна. Против неё говорят эмпирические факты, теоретические положения, например, начала термодинамики.
По материалам книги Э.А. Позднякова «Извечные загадки науки глазами дилетанта».